Η ΘΕΩΡΕΙΑ ΤΟΥ ΜΑΓΝΗΤΙΚΟΥ ΔΕΣΜΟΥ
Η ΕΝΟΠΟΙΗΣΗ ΟΛΩΝ ΤΩΝ ΧΗΜΙΚΩΝ ΔΕΣΜΩΝ
Η θεωρία του μαγνητικού δεσμού είναι μία θεωρία που προσπαθεί να εξηγήσει όλους τους χημικούς δεσμούς με την μαγνητική δύναμη. Είναι ταυτόχρονα μία προσπάθεια ενοποίησης όλων των χημικών δεσμών.
Οι προϋπάρχουσες θεωρίες των δεσμών σθένους αλλά και η κβαντική θεωρία των ατομικών και μοριακών τροχιακών είναι δύο υπέροχες θεωρίες οι οποίες όμως παρουσιάζουν κάποια ασαφή σημεία και κάποιες αδυναμίες.
Με την νέα θεωρία του μαγνητικού δεσμού δεν είναι απαραίτητος ο διαχωρισμός μεταξύ μετάλλων και αμέταλλων ή μεταλλοειδών, όπως και οι έννοιες της ηλεκτραρνητικότητας και ηλεκτροθετικότητας των στοιχείων , αλλά και οι θετικοί και αρνητικοί αριθμοί σθένους.
Με την νέα θεωρία του μαγνητικού δεσμού, θα προσπαθήσω να φωτίσω αυτά τα ασαφή σημεία και πιστεύω πως θα κάνουμε ένα βήμα πιο κοντά στην αλήθεια.
Αποδέχομαι την ύπαρξη των ατομικών και μοριακών τροχιακών, καθώς και τους δεσμούς που αναπτύσσονται μεταξύ τους. Η διαφωνία μου βρίσκεται στην αλληλεπικάλυψη των ατομικών και μοριακών τροχιακών και στο είδος του δεσμού που δημιουργείται μεταξύ τους.
Η βασική διαφοροποίηση της μαγνητικής θεωρίας του δεσμού βρίσκεται στο ότι όταν πλησιάζουν δύο ατομικά ή μοριακά τροχιακά μεταξύ τους, τότε δεν έχουμε μία αλληλεπικάλυψη των τροχιακών, αλλά μία απώθηση του ηλεκτρονικού νέφους, έτσι ώστε αυτό να συσσωρεύεται σε μία κεντρική ζώνη του κάθε ατόμου και να δημιουργείται ως εκ τούτου η εμφάνιση ενός μαγνητικού πεδίου με βόρειο και νότιο πόλο.
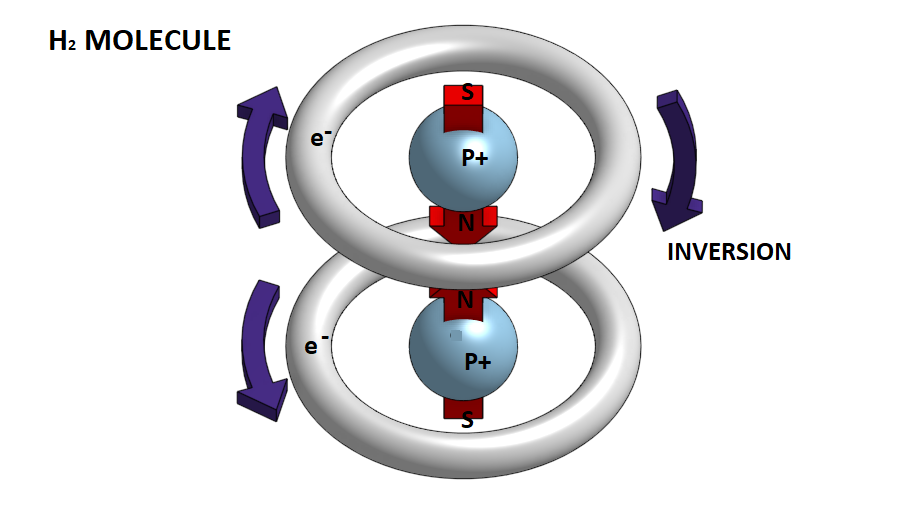
Ας εξετάσουμε την πιο απλή περίπτωση του μορίου του υδρογόνου Η2.
Οι προϋπάρχουσες θεωρίες των δεσμών σθένους αλλά και η κβαντική θεωρία των ατομικών και μοριακών τροχιακών είναι δύο υπέροχες θεωρίες οι οποίες όμως παρουσιάζουν κάποια ασαφή σημεία και κάποιες αδυναμίες.
Με την νέα θεωρία του μαγνητικού δεσμού δεν είναι απαραίτητος ο διαχωρισμός μεταξύ μετάλλων και αμέταλλων ή μεταλλοειδών, όπως και οι έννοιες της ηλεκτραρνητικότητας και ηλεκτροθετικότητας των στοιχείων , αλλά και οι θετικοί και αρνητικοί αριθμοί σθένους.
Με την νέα θεωρία του μαγνητικού δεσμού, θα προσπαθήσω να φωτίσω αυτά τα ασαφή σημεία και πιστεύω πως θα κάνουμε ένα βήμα πιο κοντά στην αλήθεια.
Αποδέχομαι την ύπαρξη των ατομικών και μοριακών τροχιακών, καθώς και τους δεσμούς που αναπτύσσονται μεταξύ τους. Η διαφωνία μου βρίσκεται στην αλληλεπικάλυψη των ατομικών και μοριακών τροχιακών και στο είδος του δεσμού που δημιουργείται μεταξύ τους.
Η βασική διαφοροποίηση της μαγνητικής θεωρίας του δεσμού βρίσκεται στο ότι όταν πλησιάζουν δύο ατομικά ή μοριακά τροχιακά μεταξύ τους, τότε δεν έχουμε μία αλληλεπικάλυψη των τροχιακών, αλλά μία απώθηση του ηλεκτρονικού νέφους, έτσι ώστε αυτό να συσσωρεύεται σε μία κεντρική ζώνη του κάθε ατόμου και να δημιουργείται ως εκ τούτου η εμφάνιση ενός μαγνητικού πεδίου με βόρειο και νότιο πόλο.
Ας εξετάσουμε την πιο απλή περίπτωση του μορίου του υδρογόνου Η2.
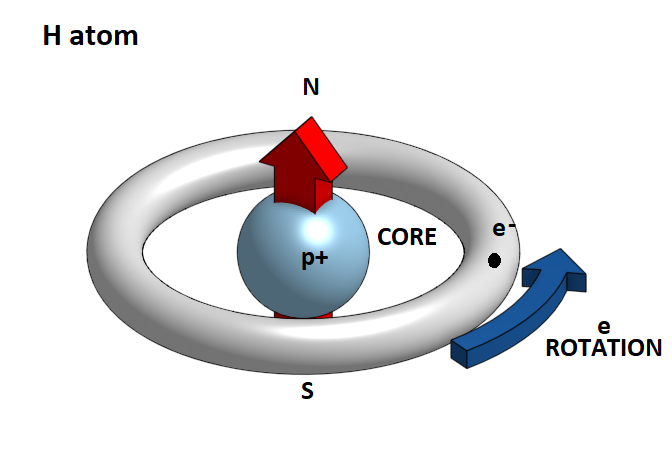
Στην περίπτωση αυτή το μοναδικό ηλεκτρόνιο δημιουργεί 1s τροχιακό. Η κατανομή του ηλεκτρονικού νέφους μοιάζει με μία σφαίρα στην οποία κινείται το μοναδικό ηλεκτρόνιο.
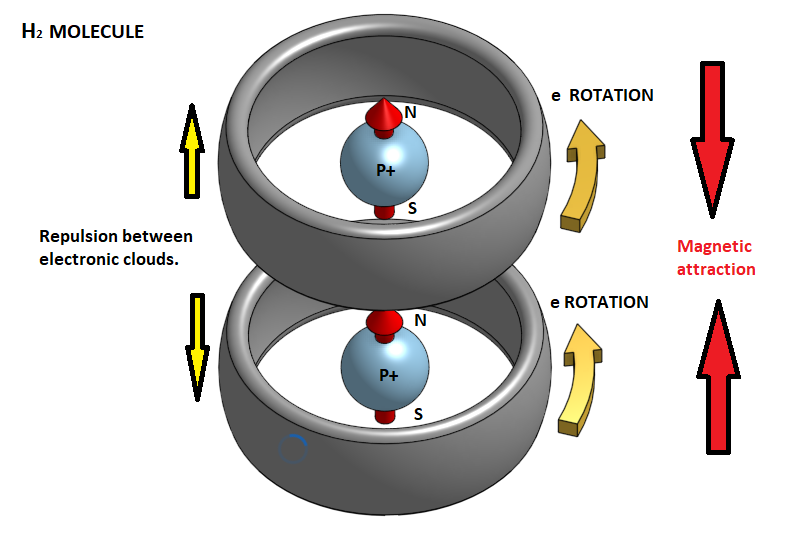
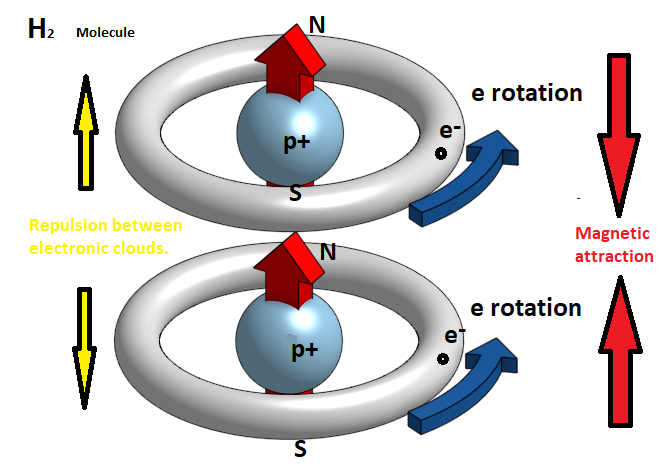
Στην πραγματικότητα το ηλεκτρόνιο διαγράφει κυκλικές τροχιές γύρω από τον πυρήνα του ατόμου και επομένως σε κάθε στιγμή δημιουργεί ένα μαγνητικό πεδίο με συγκεκριμένη πολικότητα. Επειδή όμως έχουμε συνεχόμενη εναλλαγή αυτής της περιστροφικής κίνησης, έτσι ώστε σε κάθε στιγμή το ηλεκτρόνιο να βρίσκεται σε διαφορετική τροχιά , το άτομο στο σύνολό του συμπεριφέρεται σαν ένα ουδέτερο μαγνητικά σώμα. Έτσι λοιπόν όταν δύο άτομα υδρογόνου πλησιάζουν μεταξύ τους τα ηλεκτρονικά νέφη των 1s τροχιακών που μοιάζουν με δύο αρνητικά φορτισμένες σφαίρες, απωθούνται. Αν όμως τα άτομα αναγκαστούν εξαιτίας της αύξησης της πιέσεως σε ένα αέριο, ή μιας σύγκρουσης μεταξύ τους, να πλησιάσουν το ένα στο άλλο παρά πολύ κοντά, τότε τα ηλεκτρονικά νέφη των δύο ατόμων απωθούνται και πλησιάζουν προς ένα κεντρικό σημείο του ατόμου, δημιουργώντας δύο ευδιάκριτες ζώνες περιστροφής . Ταυτόχρονα εμφανίζεται ένα προσανατολισμένο μαγνητικό πεδίο το οποίο υπερισχύει τώρα των ηλεκτροστατικών δυνάμεων και έλκει τα δύο άτομα έτσι ώστε να σχηματίσουν ένα διατομικό μόριο. Αυτό είναι το μόριο του υδρογόνου.
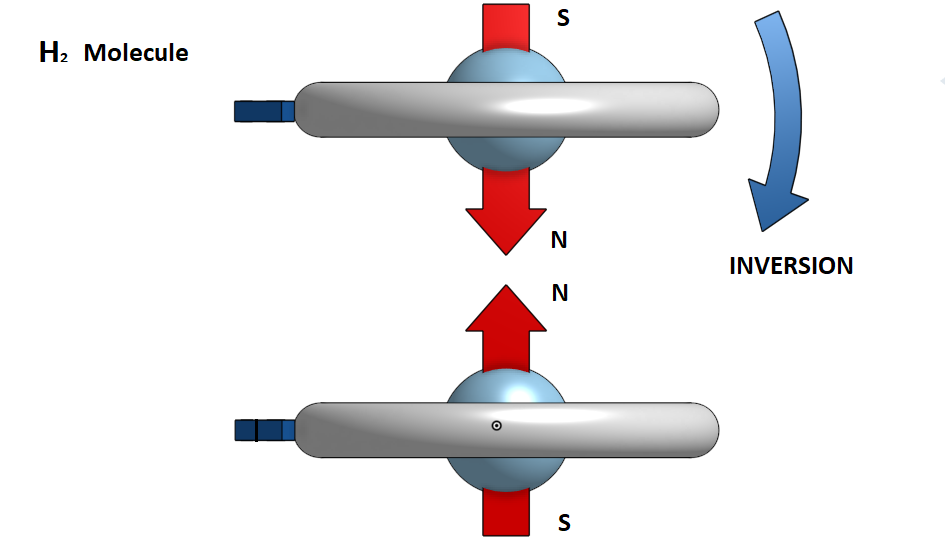
Στο μόριο του Υδρογόνου Η2 τα δύο ηλεκτρόνια είναι ομόρροπα. Στην περίπτωση που κατά την προσέγγιση των δύο ατόμων τα ηλεκτρόνια έχουν αντίθετες φορές περιστροφής τότε το ένα από τα δύο αντιστρέφεται, έτσι ώστε να γίνουν ομόρροπα και να έχουμε μαγνητική έλξη μεταξύ βορείου και νοτίου μαγνητικού πόλου.
Προφανώς για να συμβεί κάτι τέτοιο, θα πρέπει οι συνθήκες πίεσης να είναι πολύ υψηλές και η θερμοκρασία πολύ χαμηλή. Στην περίπτωση αυτή, όταν δημιουργούνται τέτοια μαγνητικά δίπολα μορίων υδρογόνου, είναι δυνατόν να ενωθούν αυτά μεταξύ τους και να σχηματιστεί ένας μεταλλικός δεσμός. Δηλαδή θα έχουμε το μεταλλικό υδρογόνο.
ΕΡΜΗΝΕΙΑ ΤΗΣ ΔΟΜΗΣ ΤΟΥ ΑΤΟΜΟΥ ΤΟΥ ΗΛΙΟΥ He.
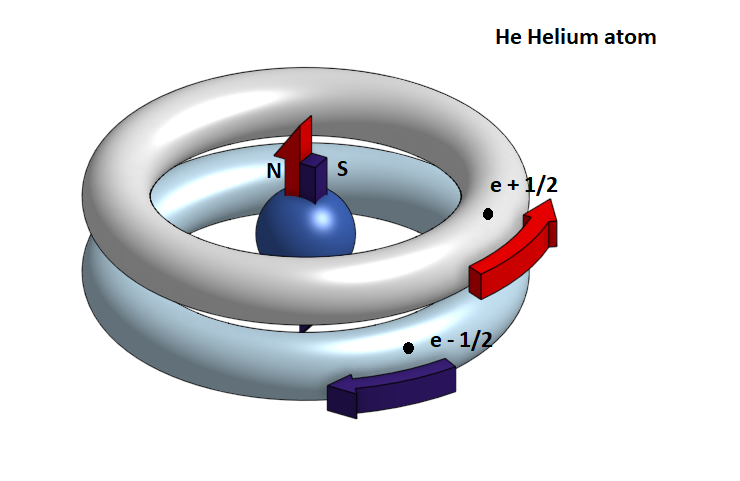
Στο άτομό του ήλιου υπάρχουν δύο πρωτόνια και δύο νετρόνια στον πυρήνα και δύο ηλεκτρόνια που περιφέρονται στη στιβάδα Κ . Τα ηλεκτρόνια αυτά έχουν αντίθετο σπιν, δηλαδή περιστρέφονται με αντίθετη φορά σε παράλληλες κυκλικές τροχιές, δημιουργώντας αντίθετα μαγνητικά πεδία που έλκονται μεταξύ τους και αλληλοεξουδετερώνονται. Έτσι το τροχιακό S που δημιουργείται, δεν εμφανίζει ένα μαγνητικό πεδίο και παραμένει μαγνητικά ουδέτερο.
Στο άτομό του ήλιου υπάρχουν δύο πρωτόνια και δύο νετρόνια στον πυρήνα και δύο ηλεκτρόνια που περιφέρονται στη στιβάδα Κ . Τα ηλεκτρόνια αυτά έχουν αντίθετο σπιν, δηλαδή περιστρέφονται με αντίθετη φορά σε παράλληλες κυκλικές τροχιές, δημιουργώντας αντίθετα μαγνητικά πεδία που έλκονται μεταξύ τους και αλληλοεξουδετερώνονται. Έτσι το τροχιακό S που δημιουργείται, δεν εμφανίζει ένα μαγνητικό πεδίο και παραμένει μαγνητικά ουδέτερο.
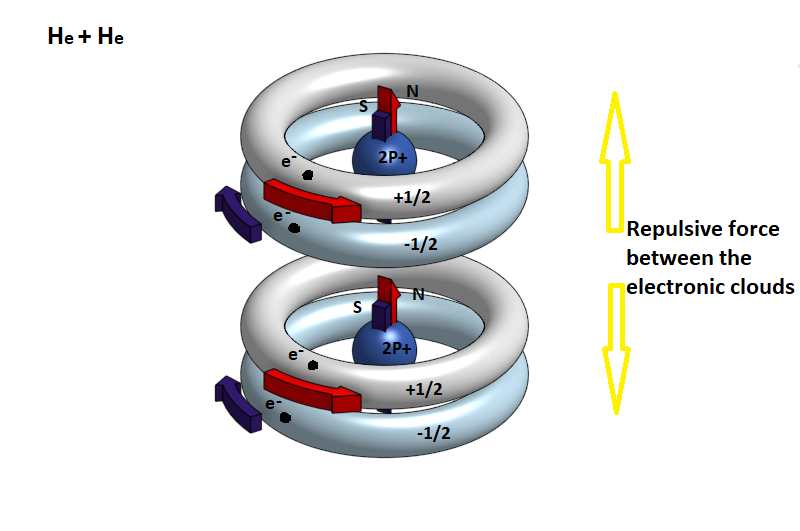
Είναι λοιπόν πολύ δύσκολο, όταν πλησιάσουν δύο άτομα ήλιου, να γίνει ένωση των ατόμων προς μόριο, διότι τα δύο ηλεκτρονικά νέφη των S τροχιακών απωθούνται ισχυρά λόγω του αρνητικού φορτίου των ηλεκτρονίων, ενώ ταυτόχρονα δεν υπάρχει μαγνητική έλξη. Για αυτό και το αέριο ήλιον είναι ένα αέριο μονατομικό που υγροποιείται πολύ δύσκολα, σε πολύ χαμηλή θερμοκρασία και είναι αδύνατον να φτάσει στη στερεά μορφή. Αυτός είναι και ο λόγος που το άτομο του αερίου ηλίου δεν σχηματίζει χημικούς δεσμούς με άλλα στοιχεία του περιοδικού πίνακα.
Ερμηνεία της δομής του ατόμου του Λιθίου Li.
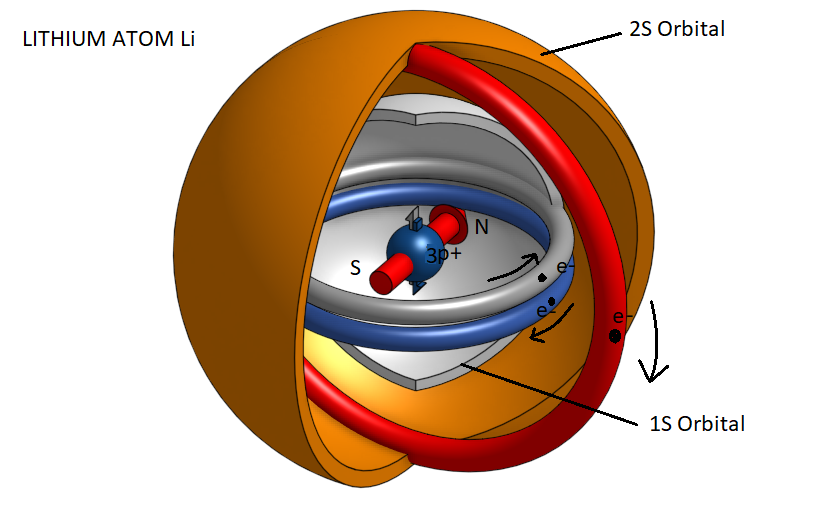
Το λίθιο είναι το τρίτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1s2 2s1. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και ένα μονήρες ηλεκτρόνιο στη στιβάδα L.
Όπως παρατηρούμε επειδή στη στιβάδα Κ υπάρχουν δύο ηλεκτρόνια με αντίθετη φορά περιστροφής, τα μαγνητικά τους πεδία αλληλοαναιρούνται. Όμως στην εξωτερική στιβάδα L όπου υπάρχει ένα ηλεκτρόνιο, δημιουργείται ένα καθαρό μαγνητικό δίπολο εξαιτίας της περιστροφής του ηλεκτρονίου. Έτσι το άτομο του λιθίου εμφανίζεται σαν ένα μαγνητικό δίπολο και έχει την ικανότητα ως εκ τούτου να σχηματίζει ισχυρούς δεσμούς με άλλα άτομα λιθίου, όπως ο μεταλλικός δεσμός στο μέταλλο του λιθίου. Αυτή η μαγνητική διπολικότητα εξηγεί επίσης και τον δραστικό του χαρακτήρα, δηλαδή την ικανότητα του λιθίου να σχηματίζει ισχυρούς δεσμούς με άλλα άτομα του περιοδικού πίνακα.
Ερμηνεία της δομής του ατόμου του Βηρυλλίου Be.
Το Βηρυλλίου είναι το τέταρτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1S2 2S1 2P1. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και δύο μονήρη ηλεκτρόνια στη στιβάδα L,το ένα στην υποστιβάδα 2S και το άλλο στην υποστιβάδα 2Px. Στη βιβλιογραφία αναφέρεται η εξής ηλεκτρονική διαμόρφωση 1S2 2S2 η οποία όμως οδηγεί σε δομή ευγενούς αερίου και προφανώς το Be θα έπρεπε να είναι αδρανές στοιχείο, κάτι που δεν ισχύει. Τα μαγνητικά δίπολα που σχηματίζονται από την περιφορά των ηλεκτρονίων 2S1 και 2P1 γύρω από τον πυρήνα, απωθούνται μεταξύ τους έτσι ώστε να ευθυγραμμιστούν με αντίθετη πολικότητα. Αυτό βέβαια θα οδηγούσε σε εξουδετέρωση της μαγνητικής ροπής των δύο διπόλων. Επειδή όμως η μαγνητική ροπή του ηλεκτρονίου 2S1 (κόκκινο βέλος) είναι μικρότερη από την μαγνητική ροπή του ηλεκτρονίου 2P1 (ανοιχτό μπλέ βέλος), τελικά η συνολική μαγνητική ροπή είναι η διαφορά τους με φορά αυτήν του ηλεκτρονίου 2P1. Επομένως το Be παρουσιάζει διπολική ροπή και μπορεί να σχηματίζει δισθενείς ενώσεις με ευθυγραμμισμένους τους δεσμούς όπως στην περίπτωση του BeCl2. Αυτοί οι δεσμοί όμως είναι μαγνητικοί. Το ζεύγος ηλεκτρονίων 1S2 δεν παρουσιάζει καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
Το Βηρυλλίου είναι το τέταρτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1S2 2S1 2P1. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και δύο μονήρη ηλεκτρόνια στη στιβάδα L,το ένα στην υποστιβάδα 2S και το άλλο στην υποστιβάδα 2Px. Στη βιβλιογραφία αναφέρεται η εξής ηλεκτρονική διαμόρφωση 1S2 2S2 η οποία όμως οδηγεί σε δομή ευγενούς αερίου και προφανώς το Be θα έπρεπε να είναι αδρανές στοιχείο, κάτι που δεν ισχύει. Τα μαγνητικά δίπολα που σχηματίζονται από την περιφορά των ηλεκτρονίων 2S1 και 2P1 γύρω από τον πυρήνα, απωθούνται μεταξύ τους έτσι ώστε να ευθυγραμμιστούν με αντίθετη πολικότητα. Αυτό βέβαια θα οδηγούσε σε εξουδετέρωση της μαγνητικής ροπής των δύο διπόλων. Επειδή όμως η μαγνητική ροπή του ηλεκτρονίου 2S1 (κόκκινο βέλος) είναι μικρότερη από την μαγνητική ροπή του ηλεκτρονίου 2P1 (ανοιχτό μπλέ βέλος), τελικά η συνολική μαγνητική ροπή είναι η διαφορά τους με φορά αυτήν του ηλεκτρονίου 2P1. Επομένως το Be παρουσιάζει διπολική ροπή και μπορεί να σχηματίζει δισθενείς ενώσεις με ευθυγραμμισμένους τους δεσμούς όπως στην περίπτωση του BeCl2. Αυτοί οι δεσμοί όμως είναι μαγνητικοί. Το ζεύγος ηλεκτρονίων 1S2 δεν παρουσιάζει καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
Ερμηνεία της δομής του ατόμου του Βορίου Β.
Το Βόριο είναι το πέμπτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1S2 2S1 2P2. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και τρία μονήρη ηλεκτρόνια στη στιβάδα L , το ένα στην υποστιβάδα 2S και τα άλλα δύο στην υποστιβάδα 2Px και 2Py. Στη βιβλιογραφία αναφέρεται η εξής ηλεκτρονική διαμόρφωση 1S2 2S2 2P1 η οποία όμως δεν μπορεί να ερμηνεύσει τον τρισθενή (±3) χαρακτήρα του Βορίου. Τα μαγνητικά δίπολα που σχηματίζονται από την περιφορά των ηλεκτρονίων 2S1 , 2P1x και 2P1y γύρω από τον πυρήνα, απωθούνται μεταξύ τους έτσι ώστε να σχηματίσουν μεταξύ τους γωνίες 120° σε επίπεδη διάταξη. Το ίδιο θα συνέβαινε και αν είχα τρεις ομόκεντρους ραβδόμορφους μαγνήτες . Το ζεύγος ηλεκτρονίων 1S2 δεν παρουσιάζει καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
Το Βόριο είναι το πέμπτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1S2 2S1 2P2. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και τρία μονήρη ηλεκτρόνια στη στιβάδα L , το ένα στην υποστιβάδα 2S και τα άλλα δύο στην υποστιβάδα 2Px και 2Py. Στη βιβλιογραφία αναφέρεται η εξής ηλεκτρονική διαμόρφωση 1S2 2S2 2P1 η οποία όμως δεν μπορεί να ερμηνεύσει τον τρισθενή (±3) χαρακτήρα του Βορίου. Τα μαγνητικά δίπολα που σχηματίζονται από την περιφορά των ηλεκτρονίων 2S1 , 2P1x και 2P1y γύρω από τον πυρήνα, απωθούνται μεταξύ τους έτσι ώστε να σχηματίσουν μεταξύ τους γωνίες 120° σε επίπεδη διάταξη. Το ίδιο θα συνέβαινε και αν είχα τρεις ομόκεντρους ραβδόμορφους μαγνήτες . Το ζεύγος ηλεκτρονίων 1S2 δεν παρουσιάζει καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
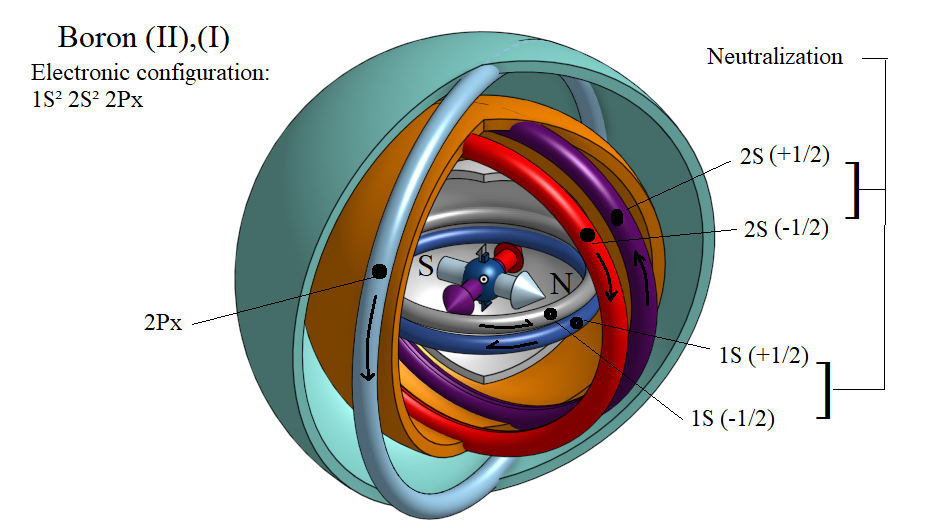
Όταν έχουμε μετάπτωση του ηλεκτρονίου 2Py στην υποστιβάδα 2S τότε έχουμε την εξής ηλεκτρονική διαμόρφωση 1S2 2S2 2P1 η οποία εξηγεί τον μονοσθενή (±1) ή δισθενή (±2) χαρακτήρα του Βορίου, γιατί το μόνο ηλεκτρόνιο που δημιουργεί μαγνητική ροπή είναι το 2P1x. Δηλαδή υπάρχει ένα ενεργό μαγνητικό δίπολο. Τα ζεύγη ηλεκτρονίων 1S2 και 2S2 δεν παρουσιάζουν καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
Ερμηνεία της δομής του ατόμου του Άνθρακα C.
Ο Άνθρακας είναι το έκτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1S2 2S1 2P3. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και τέσσερα μονήρη ηλεκτρόνια στη στιβάδα L, το ένα στην υποστιβάδα 2S και τα άλλα τρία στην υποστιβάδα 2Px ,2Py και 2Pz. Στη βιβλιογραφία αναφέρεται η εξής ηλεκτρονική διαμόρφωση 1S2 2S2 2P2 η οποία όμως δεν μπορεί να ερμηνεύσει τον τετρασθενή (±4) χαρακτήρα του Άνθρακα. Τα τέσσερα μαγνητικά δίπολα που σχηματίζονται από την περιφορά των ηλεκτρονίων 2S1 , 2P1x, 2P1y και 2P1z γύρω από τον πυρήνα, απωθούνται μεταξύ τους έτσι ώστε να σχηματίσουν μεταξύ τους γωνίες 109.5° σε 3D διάταξη. Το ίδιο θα συνέβαινε και αν είχα τέσσερις ομόκεντρους ραβδόμορφους μαγνήτες . Το ζεύγος ηλεκτρονίων 1S2 δεν παρουσιάζει καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
Ο Άνθρακας είναι το έκτο στοιχείο του περιοδικού πίνακα και έχει την εξής ηλεκτρονική διαμόρφωση 1S2 2S1 2P3. Δηλαδή έχει συμπληρωμένη στιβάδα Κ με δύο ηλεκτρόνια και τέσσερα μονήρη ηλεκτρόνια στη στιβάδα L, το ένα στην υποστιβάδα 2S και τα άλλα τρία στην υποστιβάδα 2Px ,2Py και 2Pz. Στη βιβλιογραφία αναφέρεται η εξής ηλεκτρονική διαμόρφωση 1S2 2S2 2P2 η οποία όμως δεν μπορεί να ερμηνεύσει τον τετρασθενή (±4) χαρακτήρα του Άνθρακα. Τα τέσσερα μαγνητικά δίπολα που σχηματίζονται από την περιφορά των ηλεκτρονίων 2S1 , 2P1x, 2P1y και 2P1z γύρω από τον πυρήνα, απωθούνται μεταξύ τους έτσι ώστε να σχηματίσουν μεταξύ τους γωνίες 109.5° σε 3D διάταξη. Το ίδιο θα συνέβαινε και αν είχα τέσσερις ομόκεντρους ραβδόμορφους μαγνήτες . Το ζεύγος ηλεκτρονίων 1S2 δεν παρουσιάζει καθόλου μαγνητική ροπή λόγω αλληλοεξουδετέρωσης.
Οι παραπάνω προτάσεις είναι σκέψεις του συγγραφέα που βρίσκονται σε εξέλιξη και είναι πιθανή η μελλοντική συμπλήρωση ή τροποποίησή τους. Διατηρούνται όλα τα πνευματικά δικαιώματα.
Μυτιλήνη 18-5-2019
Γιώργος Γεωργιτζίκης
Μυτιλήνη 18-5-2019
Γιώργος Γεωργιτζίκης